
Wer schlecht schläft, ist nicht nur müde – sondern langfristig auch ernsthaft gefährdet. In diesem Ratgeber erfahren Sie, was hinter dem Schlafapnoe-Syndrom steckt, wie

Wer schlecht schläft, ist nicht nur müde – sondern langfristig auch ernsthaft gefährdet. In diesem Ratgeber erfahren Sie, was hinter dem Schlafapnoe-Syndrom steckt, wie
![[object Object]](https://www.cardiopraxis.de/wp-content/uploads/2018/12/schlaganfall-sofort-erkennen-fast-test-1.webp)
Ein Schlaganfall ist ein medizinischer Notfall, der schnelles Handeln erfordert. Mit der FAST-Regel können Sie die Anzeichen eines Schlaganfalls erkennen und sofort den Notruf 112
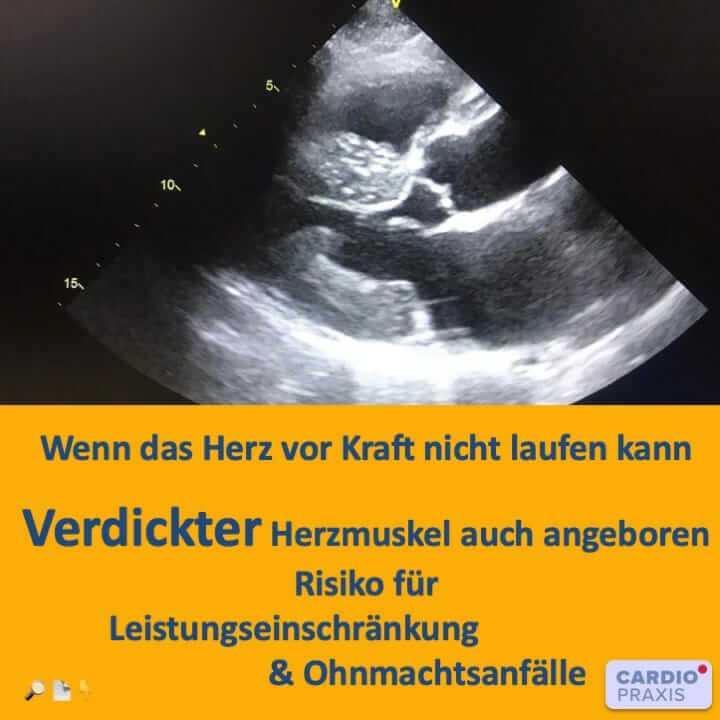
Mehr Muskelmasse! Das wünschen sich die meisten Menschen und trainieren hart dafür. Im Falle einer Herzmuskelverdickung ist dies eine gefährliche Entwicklung und muss behandelt werden.

Gelegentlich kommen Menschen zu uns in die Sprechstunde, die berichten, dass ihr Blutdruckmessgerät einen sehr niedrigen Puls angezeigt hat. Oder Herzschrittmacher-Patienten fühlen am Handgelenk einen

Eine plötzliche Ohnmacht ist ein angstauslösendes Ereignis: Dahinter können sich ganz unterschiedliche Krankheitsbilder verbergen. Eine sorgfältige Anamnese und Diagnostik ist hier entscheidend, um das individuelle

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten

Sie leiden an Bluthochdruck oder Vorhofflimmern und sind sich unsicher, ob Sie ein regelmäßiges Ausdauertraining durchführen können oder sogar sollen. Hier erfahren Sie mehr.
Normalerweise spüren wir unseren Herzschlag nicht. Beim Herzstolpern nehmen wir Unregelmäßigkeiten wahr. Häufig bemerken wir Aussetzer, als ob ein Herzschlag fehlt. Dies verunsichert uns, der

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten

Anfallsartiges Herzrasen betrifft auch gesunde Menschen. Typisch sind ein plötzlicher Beginn und ein Ende, als ob man einen Lichtschalter an, beziehungsweise ausknipst. Solches Herzrasen kann

Fast jedem, der regelmäßig Medikamente einnehmen muss, ist es schon mal passiert: die Tablette einfach vergessen! Gerade bei Herzmedikamenten gilt: Auf keinen Fall die doppelte

Wir alle wissen, ein Herzinfarkt ist gefährlich. Aber was passiert dabei eigentlich und warum sterben Menschen plötzlich am Herzinfarkt? Wir klären auf. Sie sehen gerade

In der Kardiologie empfehlen wir unseren Patienten sowohl Herzschrittmacher als auch Defibrillatoren. Aber was ist eigentlich der Unterschied zwischen den Geräten und wann empfehlen wir

Wir Kardiologen empfehlen ja gerne Sport. Aber wie ist das, wenn ich einen implantierbaren Defibrillator habe? Darf ich dann Sport treiben? Was muss ich beachten?
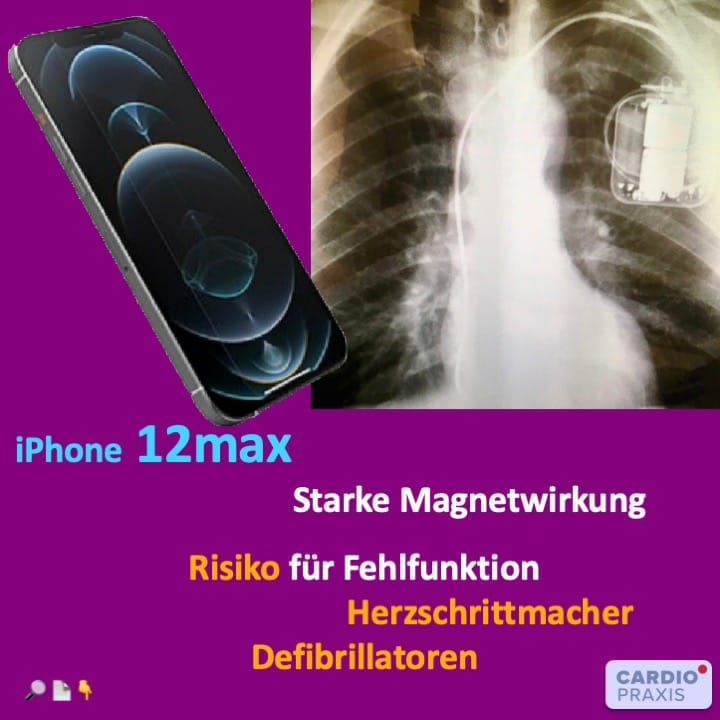
Wer will es nicht haben, das neue iPhone 12? Aber aufgepasst, das neue iPhone 12 hat einen stärkeren Magneten als Vorgängermodelle. Dies hat Bedeutung für

Was hat ein Gelenkersatz mit dem Herzen zu tun? Wussten Sie, dass es bei jedem 5. Patienten nach Eingriffen an Knie oder Hüfte zu einem

Erkältung überstanden aber immer noch schlapp? Und besonders bei Belastung kommt Ihr Körper jetzt viel schneller an seine Grenzen? Symptome wie Herzrasen oder Luftnot nach
Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten
Erhalten Sie unseren Kardiologie-Newsletter einmal im Monat mit allen wichtigen Updates rund um kardiologische Themen. Bleiben Sie stets informiert. Für Ihr Herz und Ihre Gesundheit!
Liebe Patientinnen und Patienten,
am kommenden Montag, den 14. Juli 2025 schließen unsere beiden Praxen in Düsseldorf und Meerbusch bereits um 13.00 Uhr.
Ab Dienstagmorgen sind wir wieder wie gewohnt für Sie erreichbar.
Wir bitten um Ihr Verständnis.
Ihr Team der Cardiopraxis
ab Dienstag, 30. Juli 2024 werden wir unsere Terminbuchungssoftware von Samedi auf Doctolib umstellen. Zusätzlich freuen wir uns, Ihnen die Einführung unserer neuen Online-Rezeption anzukündigen. Mit diesen Veränderungen können wir unseren Service für Sie weiter verbessern.
Um Ihnen den Übergang so reibungslos wie möglich zu gestalten, haben wir intensive Vorbereitungen getroffen. Alle bereits vereinbarten Termine werden automatisch in Doctolib übertragen! Sie müssen sich also keine Sorgen machen – kein geplanter Termin geht verloren, ganz gleich ob Sie diesen online via Samedi oder bei uns direkt gebucht haben.
Dank unserer neuen und innovativen Online-Rezeption, die Sie auf unserer Website unten rechts finden, erreichen Sie uns auf direktem Wege auch außerhalb der Sprechzeiten und umgehen so die Wartezeit am Telefon. Nebst Terminvereinbarungen können Sie auf diesem Wege unter anderem auch unkompliziert Rezepte und Befunde anfordern.
Falls Sie Fragen oder Bedenken bezüglich der Umstellung haben, stehen wir Ihnen selbstverständlich zur Verfügung. Unser Praxisteam ist darauf vorbereitet, Ihnen zu helfen. Weitere Informationen zu Doctolib erhalten Sie hier in unserer Cardiothek.

Sie müssen den Inhalt von reCAPTCHA laden, um das Formular abzuschicken. Bitte beachten Sie, dass dabei Daten mit Drittanbietern ausgetauscht werden.
Mehr InformationenSie müssen den Inhalt von reCAPTCHA laden, um das Formular abzuschicken. Bitte beachten Sie, dass dabei Daten mit Drittanbietern ausgetauscht werden.
Mehr Informationen