
Übergewicht ist ungesund und ein erheblicher Risikofaktor für Erkrankung und Tod. Ganz entscheidend ist aber auch, wie das Übergewicht verteilt ist, das heißt, wo die

Übergewicht ist ungesund und ein erheblicher Risikofaktor für Erkrankung und Tod. Ganz entscheidend ist aber auch, wie das Übergewicht verteilt ist, das heißt, wo die

Hitzestress belastet Herz und Kreislauf enorm. Blutdruckschwankungen, Vorhofflimmern und Herzinfarkt drohen. Mit einfachen Maßnahmen wie ausreichend Trinken, leichte Kleidung, Hitze meiden und Medikamente anpassen können

Leiden Sie unter Herzstolpern, Herzrasen oder Blutdruckschwnakungen nach dem Essen bestimmter Lebensmittel? Möglicherweise steckt eine Histaminintoleranz dahinter. Erfahren Sie hier, was die Ursachen und Symptome

Fragen Sie sich, ob das Nahrungsergänzungsmittel Omega-3 für Sie das gesund ist. Hier erfahren Sie, welche Dosis die richtige ist und wer ein besonders hohes

Die Bedeutung der Trinkmenge wird unterschätzt. Trinken hat eine hohe Relevanz für Ihre Herz-Kreislaufgesundheit. Hier erfahren Sie mehr zur richtigen Trinkmenge und Symptomen eines Flüssigkeitsmangels.

Asthma-Sprays können selbst Luftnot verursachen. Warum das so ist, wie wir das erkennen können und was dann zu tun ist, das erfahren Sie hier.

Sie überlegen sich, ob Sie zu einem Kardiologen beziehungsweise zu einer Kardiologin gehen sollen. Vielleicht hat Ihnen auch Ihr Hausarzt empfohlen eine fachärztliche kardiologische Untersuchung

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten
Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei

COVID-19 – Notfall Herzinfarkt, Schlaganfall – 112 immer verständigen Die COVID-19 Virusepidemie führt zu einer deutlichen Mehrbelastung der Notaufnahmestationen der Krankenhäuser. Folglich stellen sich zahlreiche

COVID-19 – Herzrhythmusstörungen – Vorhofflimmern und andere bei Corona Virusinfektion COVID-19 – Herzrhythmusstörungen sind ein relevantes medizinische Problem, denn die Corona Virusinfektion betrifft nicht nur die Lunge,

Holiday Heart Syndrom – was ist das? Im Jahr 1978 hat Philipp Ettinger den Begriff Holiday Heart Syndrom erstmalig beschrieben. Die Grundlage dafür war
Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten
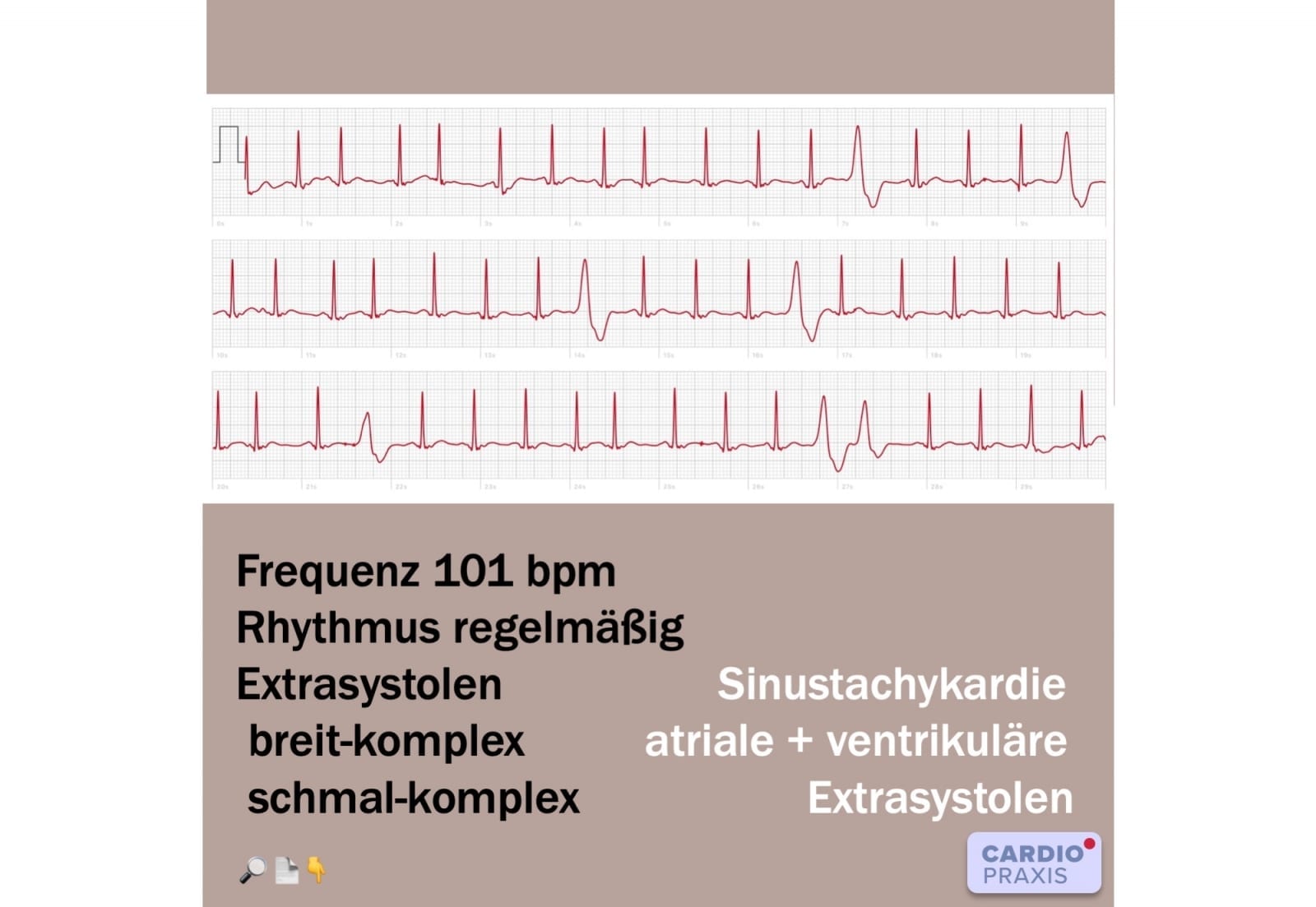
, Herzrasen nach dem Mittagessen – Herzrhythmusstörungen durch Histamin Vorgeschichte Bei einem 57-jährigen Mann ist seit der Kindheit eine saisonale Allergie bekannt. Seit dem jungen

Bier auf dem Oktoberfest – Risikofaktor für Herzrhythmusstörungen Seit 1810 findet in München das Oktoberfest statt. Ursprünglich als Feierlichkeit anlässlich der Hochzeit von Kronprinz

Apple Watch und AliveCor – 1-Kanal EKG zur Vorbeugung eines Schlaganfalls Mit der Apple Watch von Apple und Kardia Band bzw. Kardia Mobile von

Herzstolpern, Herzrasen – Warum ein 1-Kanal-EKG mit dem Smartphone? Die EKG-Funktion von Smartphones entweder in Verbindung mit einer Smartwatch oder anderen Geräten zur Ableitung wird
Erhalten Sie unseren Kardiologie-Newsletter einmal im Monat mit allen wichtigen Updates rund um kardiologische Themen. Bleiben Sie stets informiert. Für Ihr Herz und Ihre Gesundheit!

Unsere Schließzeiten über die Feiertage
Am 23. Dezember haben wir in Meerbusch noch bis 14 Uhr und in Düsseldorf bis 17 Uhr geöffnet.
Zwischen dem 24. Dezember und 01. Januar sind unsere beiden Praxen geschlossen.
Wir wünschen Ihnen schöne Feiertage und alles Gute für 2026!

Liebe Patientinnen und Patienten,
am Rosenmontag, dem 16. Februar 2026, bleiben unsere Praxen in Düsseldorf und Meerbusch ganztägig geschlossen.
Ab Dienstag um 8.00 Uhr sind wir wieder für Sie erreichbar.
Liebe Grüße
Ihr Cardiopraxis-Team
ab Dienstag, 30. Juli 2024 werden wir unsere Terminbuchungssoftware von Samedi auf Doctolib umstellen. Zusätzlich freuen wir uns, Ihnen die Einführung unserer neuen Online-Rezeption anzukündigen. Mit diesen Veränderungen können wir unseren Service für Sie weiter verbessern.
Um Ihnen den Übergang so reibungslos wie möglich zu gestalten, haben wir intensive Vorbereitungen getroffen. Alle bereits vereinbarten Termine werden automatisch in Doctolib übertragen! Sie müssen sich also keine Sorgen machen – kein geplanter Termin geht verloren, ganz gleich ob Sie diesen online via Samedi oder bei uns direkt gebucht haben.
Dank unserer neuen und innovativen Online-Rezeption, die Sie auf unserer Website unten rechts finden, erreichen Sie uns auf direktem Wege auch außerhalb der Sprechzeiten und umgehen so die Wartezeit am Telefon. Nebst Terminvereinbarungen können Sie auf diesem Wege unter anderem auch unkompliziert Rezepte und Befunde anfordern.
Falls Sie Fragen oder Bedenken bezüglich der Umstellung haben, stehen wir Ihnen selbstverständlich zur Verfügung. Unser Praxisteam ist darauf vorbereitet, Ihnen zu helfen. Weitere Informationen zu Doctolib erhalten Sie hier in unserer Cardiothek.

Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von YouTube. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie müssen den Inhalt von reCAPTCHA laden, um das Formular abzuschicken. Bitte beachten Sie, dass dabei Daten mit Drittanbietern ausgetauscht werden.
Mehr InformationenSie müssen den Inhalt von reCAPTCHA laden, um das Formular abzuschicken. Bitte beachten Sie, dass dabei Daten mit Drittanbietern ausgetauscht werden.
Mehr Informationen